


возможностей при заболеваниях печени Щербинина М.Б., д.мед.н., профессор, Президент „Украинской ассоциации по изучению заболеваний печени”, Майкова Т.В., д.мед.н., профессор Семашко А.В., к.мед.н. Медицинский центр амбулаторного обслуживания детей и взрослых «Поликлиника Св. Антипы», Днепропетровск Одной из основных задач, стоящих перед современным клиницистом, является рациональный выбор исследований, позволяющих провести максимально точную диагностику. При заболеваниях печени вне зависимости от этиологии особую актуальность имеет определение морфологической стадии фиброза печени (ФП), а также дифференцирование очаговых образований ее ткани. Это необходимо для прогнозирования течения и оценки стабилизации патологических процессов на фоне проводимой терапии. С целью изучения выраженности ФП в количественном эквиваленте (кПа) в начале 2000 гг была разработана непрямая ультразвуковая эластометрия с использованием аппарата Fibroscan французской фирмы Echosens, именуемая в специальной литературе «transient еlastography» (ТЕ). ТЕ представляет собой узкоспециализированную методику, применяемую только для определения эластичности ткани печени [1]. Ряд выводов, сделанных на основании многолетнего опыта использования ТЕ при патологии печени, подробно изложены в докладе на ресурсе www.elsevier.ru/WNH. В дальнейшем визуализация морфологической структуры печени совершенствовалась с обособлением 2-х видов методик: эластографии сдвиговой волны (acoustic radiation force impulse (ARFI) – акустическая импульсно-волновая эластография [2], и статической (компрессионной) эластографии [3]. Развитием последней занимается несколько ведущих компаний – производителей ультразвукового оборудования Premium-класса, каждая из которых запатентовала для нее свое название: у Hitachi – это Real-Time Elastography (RTE) – эластография в реальном времени; у Toshiba – лаконично Elastography; Ultrasonix обозначает методику Free Hand RTE. Не вдаваясь в терминологическую дискуссию, подчеркнем, что это синонимические названия одной и той же методики. Далее в статье мы обозначаем ее RTE. На базе Медицинского центра амбулаторного обслуживания детей и взрослых «Поликлиника Св. Антипы» создан единственный в Днепропетровске центр диагностики и лечения сложных заболеваний печени под руководством д.мед.н., профессора, Президента Украинской ассоциации по изучению болезней печени М.Б. Щербининой. При заболеваниях печени вне зависимости от этиологии особую актуальность имеет определение морфологической стадии фиброза (ФП), а также дифференцирование очаговых образований ее ткани. RTE – эластография является новым методом диагностики ранних стадий цирроза печени, контроля хода лечения, а также диагностики ранних стадий онкологических заболеваний печени. Исследование проводят опытные врачи сонологи на ультразвуковом сканере Premium-класса Sonix Touch, канадской компании Ultrasonix. Применение RTE для исследования эластических свойств глубоко расположенных органов является относительно новым. Из-за недостаточного количества в нашей стране техники для ее проведения на сегодняшний день украинские врачи нечетко понимают суть и диагностические возможности метода. Исходя из этого, в данной статье нам хотелось бы ознакомить широкую аудиторию врачей с методикой RTE, ее потенциалом в диагностике заболеваний печени и привести описание нескольких клинических случаев собственных наблюдений. RTE является разновидностью ультразвукового метода с направленностью изучения эластичности ткани в режиме реального времени. Принципиальным отличием методик ARFI, RTE и ТЕ является использование двумя первыми прямой визуализации предмета исследования. Этого лишена методика ТЕ, выполняющаяся путем «слепого» наведения сигнала. Кроме того, и ARFI, и RTE позволяют изучать не только диффузные поражения печени, но и с успехом решать вопросы ее очаговой патологии, а также других органов брюшной полости (поджелудочной железы и почек, надпочечников, органов малого таза). Сравнительная характеристика указанных методик представлена в табл.1.
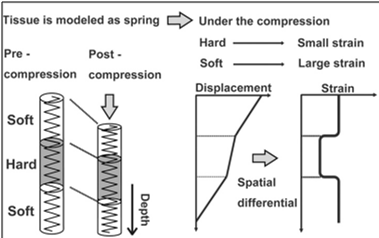
Рис. 1. Основа метода RTE заключается в анализе и визуализации распределения деформации путем статической компрессии на поверхность тела; это иллюстрируется в виде «модели пружины» [3] Табл. 1. Сравнительная характеристика основных методик ультразвукового исследования эластичности ткани при диффузных заболеваниях печени [4-8]
|
Критерий сравнения |
Название методики эластометрии / эластографии | ||
|
ТЕ, аппарат FibroScan, Echosens |
ARFI, аппараты Siemens, Phillips |
RTE, · аппараты Hitachi, Toshiba, Ultrasonix | |
|
F≥ 2 (клинически значимые степени фиброза) | |||
|
Чувствительность (%) |
64.9 |
78.9 |
64.9 |
|
Специфичность (%) |
70.6 |
58.8 |
35.3 |
|
F= 4 (фиброз / цирроз) | |||
|
Чувствительность (%) |
81.0 |
90.5 |
81.0 |
|
Специфичность (%) |
64.2 |
66.0 |
64.2 |
|
Преимущества и ограничения, области применения, влияющие факторы | |||
|
Воспроизводимость |
Высокая |
Высокая |
Высокая |
|
Повторяемость |
Средняя |
Высокая |
Высокая |
|
Ограничения (приводят к возрастанию погрешности) |
Узкие межреберные промежутки, ожирение III – IV ст., асцит, вторично сморщенная печень, выраженный холестаз, острый гепатит, высокий уровень портальной гипертензии |
Ожирение III – IV ст., асцит, выраженный холестаз, острый гепатит
|
Выраженные нарушения сердечного ритма. Для линейного датчика – глубина исследования не более 5 см, для конвексного датчика – без ограничений. |
|
Область применения |
Исследования диффузных процессов печени. Исследование селезенки в стадии апробации. |
Диагностическое применение ультразвука, включая диффузные и очаговые поражения органов. |
Диагностическое применение ультразвука, включая диффузные и очаговые поражения органов. Контроль проведения инвазивных диагностических (пункционная биопсия) и лечебных (радиочастотная, лазерная абляция) Интраоперационные исследования линейным датчиком. |
|
Недостатки |
«Слепой» метод наведения импульс – датчика, отсутствие синхронного В – режима. Узкоспециализированный метод, без возможности расширения области использования. Наибольшее число ограничений, влияющих факторов. Наиболее высокая себестоимость исследования |
Отсутствуют инструменты для интраоперационных и эндоскопических исследований (поджелудочная железа, печень). |
Невозможность выражать результат исследования в абсолютных показателях плотности – кПа. |
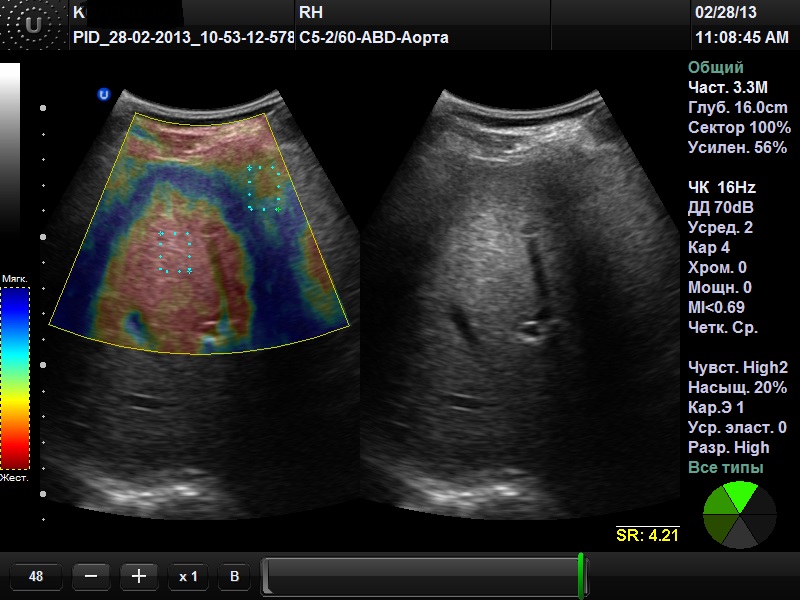 Рис. 2. RTE от 28.02.2013, участок фиброза печени с ЕSR = 4,21
Рис. 2. RTE от 28.02.2013, участок фиброза печени с ЕSR = 4,21
Технология исследования базируется на выявлении признаков поражения печени в В–режиме, затем проводится исследование в режиме RTE. Принцип RTE для печени обосновывается с позиции физической «модели пружины» (рис. 1) и законов Кросс – корреляционного анализа эластических свойств ткани. При исследовании печени применяется «Heartbeat методика» компрессионного воздействия, т.е. ритмичная физиологическая компрессия, которой, как и другие внутренние органы, подвергается печень вследствие пульсации сердца и расположенных рядом крупных артериальных сосудов. При этом мягкие части ткани печени деформируются в большей степени, плотные – в меньшей. Отраженные эхо-сигналы улавливаются датчиком и используются компьютером для вычисления перемещения участков ткани органа, после чего на экран выводится изображение распределения его деформации в режиме цветового картирования. Дополнительная механическая ручная компрессия не используется. Адекватность нажатия датчиком в проекции печени на передней брюшной стенке, производимого врачом-сонологом, контролируется соответствующим индикатором на экране монитора (зеленая круглая диаграмма в правом нижнем углу экрана, см. рис. 2 - 6). Это гарантирует получение изображения с минимальным количеством артефактов. Каждый участок эластографического изображения с другим числовым значением эластичности связан с тем или иным состоянием ткани (нормальная ткань, разные степени фиброза, очаговые образования паренхимы печени и т.д.) и визуально идентифицируется соответствующим цветом. Например, в ультразвуковом сканере фирмы Ultrasonix (Канада) наименее эластичные ткани окрашены в тёмно-красный цвет, ткани средней эластичности – в желто-зеленый, эластичные ткани - в цвета сине-голубого спектра. Просматривая цветовую гамму изображения, судят об однородности структуры печени, наличии, локализации и особенностях выявленных изменений. Достоинством RTE, облегчающим трактовку результатов, является синхронное выполнение визуализации печени в серошкальном В-режиме изображения в реальном времени и режиме цветового картирования этих же участков ткани (на экран выводятся одновременно оба изображения, см. рис. 2-6). RTE позволяет оценивать эластичность ткани печени цветовой кодировкой по шкале Fujimoto K. et al. [9] и количественными расчетными показателями относительной эластичности ткани - elastic stran ratio (ЕSR ) - в, так называемых, зонах интереса - region of interest (ROI): участка А, проблемного с точки зрения диагностики (ROI-А), и участка-эталона В (ROI-В). Коэффициент эластичности ЕSR представляет собой отношение значений B/A, количественно характеризующее эластичность проблемного участка. В качестве контрольной точки ROI-В выступает, как правило, расположенный рядом с ROI-А участок печеночной вены. Референтные значения печеночных вен выбраны потому, что их эластичность не меняется с возрастом. Печеночные вены также не подвержены трансформациям, связанным с повышением или понижением плотности стенки, например, при артериосклерозе, и на всем протяжении болезни печени, даже при фиброзной трансформации ее паренхимы [3]. По результатам исследования высчитывается наиболее важный для врача клинициста показатель среднего значения – ЕSR mean. При хронических заболеваниях печени врач ориентируется на данный показатель, оценивая динамику состояния ее паренхимы без и на фоне проводимой терапии. По мнению ученых, методика RTE легко воспроизводима, не зависит от ограничений по состоянию пациентов, как ТЕ, и что наиболее ценно – показатели RTE имеют четкую корреляцию с морфологическими стадиями шкалы Metavir. Согласно общепринятой шкале Metavir проводится следующая морфологическая оценка стадии ФП. Стадия F0 – отсутствие фиброза, F1 – расширение портальных трактов без формирования септ, F2 – портальный фиброз в сочетании с единичными септами, F3 – портальный фиброз в сочетании с множественными септами без ложных долек, F4 – цирроз печени. Повышение уровня ЕSR позитивно коррелирует с повышением плотности печени по данным пункционной биопсии (r = 0.82, р = 0,001), и соотносится с распределением стадий фиброза по шкале Метаvir. Результаты соответствия данных RTE и степени фиброза по шкале Метаvir выглядят следующим образом: F1 – среднее значение 2.21 (диапазон: 1.94 - 2.70); F2 – среднее значение 2.69 (диапазон: 2.29 -2.97); F3– среднее значение 3.42 (диапазон: 3.07 - 3.65); и F4– среднее значение 4.66 (диапазон: 4.40 -4.93) [3]. Также данные, полученные с помощью ЕSR, коррелируют с данными оценки фиброза с помощью исследований показателей гиалуроновой кислоты, коллагена IV типа, APRI – индекса (aspartate aminotransferase–to–platelet ratio index), FibroIndex, лабораторных методик Forns score и Hepascore соответственно: 0.95, 0.32, 0.73, 0.76, 0.76, 0.87 и 0.70. При этом, оценка стадии фиброза F1 методом RTE выявила большую чувствительность по сравнению с серологическим методом [3]. В последние 3 года усилия ученых были направлены на создание технических способов, позволяющих повысить информативность качественного компонента RTЕ – цветового паттерна. Объективизации цветовых характеристик позволили достигнуть разработки в области «Computer-aided artificial neural network dynamic analysis» – программных средств «off – line» оценки полученного изображения. К ним относятся программа «Statistica Neural Networks v. 4.0 E» (производство StatsoftInc, Tulsa, Okla), а также программа для обработки и анализа изображений «ImageJ Software» (производство NIH, Bethesda, MD. ImageJ). Последняя подготовлена сотрудниками Национального Института Здоровья (США) и распространяется как общественное достояние без лицензионных ограничений. Программы охватывают широкий круг задач обработки изображений, что открывает новые возможности для достижения исследовательских целей. В частности, дискретный анализ «плотности и географии расположения» 256 – пиксельной цветовой палитры позволяет осуществить виртуальный гистосканинг паренхимы печени. Именно эта технология расценивается как инструмент неинвазивного изучения диффузных патологических процессов органа. В случае выявления в В – режиме очагового поражения печени врач-сонолог с помощью RTE оценивает очаг с позиции «доброкачественное / злокачественное образование», проводит предположительную оценку гистоструктуры очага и определяет область биопсии при наличии показаний. Доказано, чем ниже эластичность новообразования, тем более злокачественным оно является. Для качественной оценки очагового образования применяется шкала Tsukuba Elasticity Score pattern, которая уже на этом этапе исследования позволяет предположить доброкачественный или злокачественный характер образования. Преобладание синего цвета соответствует эластичной («мягкой»), а значит – доброкачественной ткани. Выявление пестрого неоднородного паттерна с преобладанием красного цвета или преимущественно красный паттерн присущ неэластичной («жесткой»), а, следовательно, злокачественной ткани. В случае очагового образования для расчета коэффициента эластичности ЕSR как участок-эталон ROI-В обычно используется неизмененная область самого органа. Значения коэффициента эластичности ЕSR в очаге поражения позволяет также с высокой степенью вероятности предположить гистологические особенности образования. Коэффициент эластичности ЕSR выше 2,88 является основанием для трактовки очагового образования как злокачественного. В отличие от прежних представлений гепатоцеллюлярную карциному (ГЦК) относят к крайне распространенным опухолям. Причина этого заключается в росте числа пациентов с вирусиндуцированным циррозом печени. В любом случае цирроз печени независимо от этиологии рекомендуется рассматривать как предраковое состояние. Особенно высок риск у лиц с высокой активностью процесса и повышением концентрации ?–фетопротеина. Для максимально ранней диагностики ГЦК эти пациенты должны регулярно обследоваться, в том числе используя RТЕ. Особая ценность RТЕ заключается в том, что методика с высокой чувствительностью выявляет изоэхогенные очаговые образования независимо от степени их васкуляризации, диагностика которых затруднена не только для рутинного УЗИ, но и в ряде случаев – при выполнении контрастной компьютерной томографии. Это касается, например, метастазов в паренхиму печени. При исследовании региональных лимфатических узлов RTE позволяет провести дифференциальную диагностику между их воспалительными и метастатическими изменениями [10]. Поэтому методику можно использовать для уточнения стадии злокачественного процесса органов гепато-панкреато-дуоденальной зоны. Таким образом, современная генерация ультразвукового оборудования при выполнении RTE позволяет осуществлять как качественный, так и количественный анализ эластичности ткани исследуемого органа. Методика RTE расширяет наши диагностические возможности, выгодно отличая RTE от ТЕ (фибросканирования). RTE дает четкую оценку степени фиброза / цирроза печени по шкале Метаvir. Принципиально важным является определение ранних стадий заболевания, а также фиксирование показателя среднего значения «ESR mean», изменения которого при последующих исследованиях дает возможность оценить положительную или отрицательную динамику состояния паренхимы печени, а также оценить эффективность проводимого лечения. Показатели RTE являются важным дополнительным критерием оценки характера изменений в тканях различных органов. На практике это позволяет не только с большой вероятностью заподозрить опухолевый или метастатический процесс, но и уточнить область взятия биопсийного материала с целью морфологической верификации, а также оценить полноту проведения хирургического вмешательства, (например, удаление опухоли или разрушение метастазов в печени при радиочастотной абляции. Ниже приводим описание нескольких клинических случаев собственных наблюдений. RTE печени проведено по стандартной методике [3] на ультразвуковом сканере Premium-класса Sonix Touch, канадской компании Ultrasonix (e-mail: doctrina@ua.fm). Клинический случай 1. Пациент К., 44 г., прошел противовирусную терапию (ПВТ) (пегинтрон+ребетол) по поводу хронического вирусного гепатита С (HCV), генотип 1b. Показатели общеклинических анализов, печеночного комплекса, данные УЗИ органов брюшной полости – в пределах нормы. Заключение RTЕ (рис. 2) от 28.02.13 (6 мес. от начала ПВТ): диапазон колебаний индекса ЕSR 2,15 -4,21, ESR mean 3,15 что соответствует степени фиброза F3-F4 по шкале Метаvir. Заключение RTE (рис. 3) от 22.08.13 (12 мес. от начала ПВТ): диапазон колебаний индекса ESR 1,08 -2,42, ESR mean 1,69, что соответствует степени фиброза F1-F2 по шкале Метаvir.
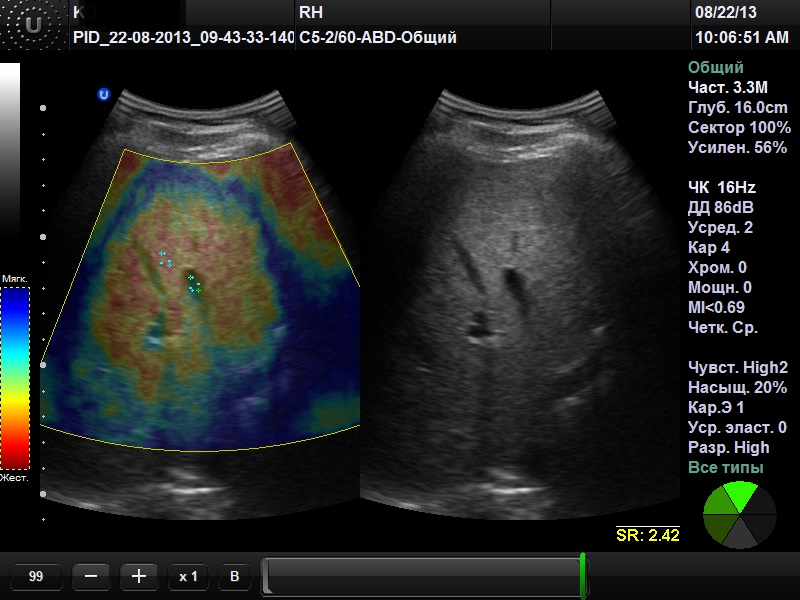 Рис. 3. RTE от 15.08.2013, участок фиброза печени с ЕSR = 2,42
Рис. 3. RTE от 15.08.2013, участок фиброза печени с ЕSR = 2,42
Снижение степени вирусного ФП сегодня является доказанным фактом. Наиболее часто и более выраженные изменения ФП наблюдаются при полной эрадикации вируса гепатита С (формирование стойкого вирусологического ответа, который остается главной целью ПВТ.) Таким образом, поскольку устранен этиологический фактор, поражение печени регрессирует, что подтверждено RTЕ. Клинический случай 2. Женщина, 52 г., с астеническим синдромом многократно обследовалась без установления точного диагноза. Показатели общеклинических анализов, печеночного комплекса в течение нескольких последних лет всегда соответствовали норме. Данные УЗИ органов брюшной полости в динамике без особенностей. Заключение RTЕ от 23.02.13 (рис. 4): диапазон колебаний индекса ESR 2,3 – 2,8, ESR mean 2,47, что соответствует степени фиброза F2-F3 по шкале Метаvir.
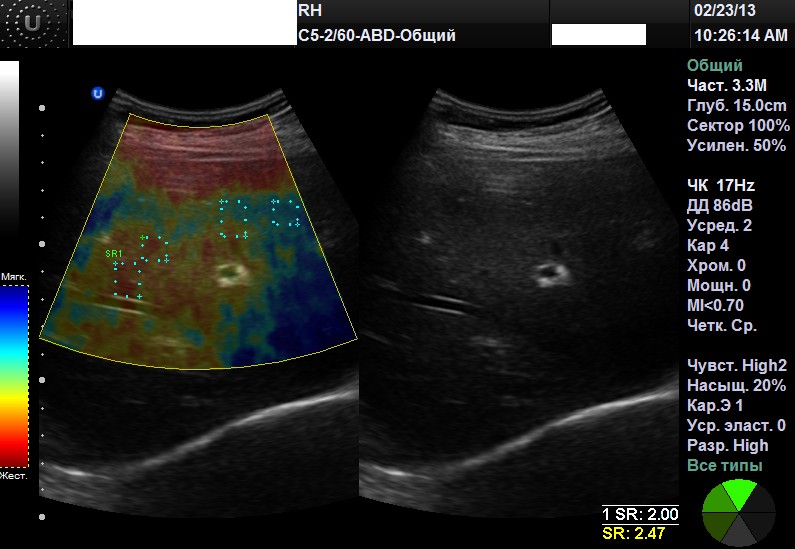
Рис. 4. RTЕ от 23.02.13, степень фиброза F2 – F3 по шкале Метаvir Направлена на исследование крови по поводу хронических вирусов гепатита. Выявлено наличие РНК- HCV, генотип 1b, вирусная нагрузка 2,1 х 106 копий/мл (7,7 х105 МЕ/мл). По мнению экспертов EASL, всех пациентов с компенсированным HCV, ранее не получавших лечения, которые желают лечиться и не имеют противопоказаний, следует рассматривать как кандидатов на противовирусную терапию, независимо от исходного уровня трансфераз (АЛТ). Лечение рекомендовано пациентам с выраженным фиброзом (оценка по шкале Metavir F3-F4) и строго рекомендовано пациентам с умеренным фиброзом (F2 по шкале Metavir). Таким образом, хронический вирусный гепатит С протекал без изменения лабораторных и ультразвуковых данных. Выявление степени фиброза F2-F3 по шкале Метаvir позволило заподозрить эту инфекцию, назначить целенаправленное исследование, установить диагноз и начать антивирусную терапию. Клинический случай 3. Женщина, 56 лет, при УЗИ печени обнаружены множественные очаговые образования печени с низкой васкуляризацией в допплеровском режиме, на RTЕ - цветовой паттерн неоднородного типа с красным спектром. Показатель ЕSR в очагах от 4,35 до 6,10. Заключение: множественные метастазы печени, рекомендовано проведение биопсии.
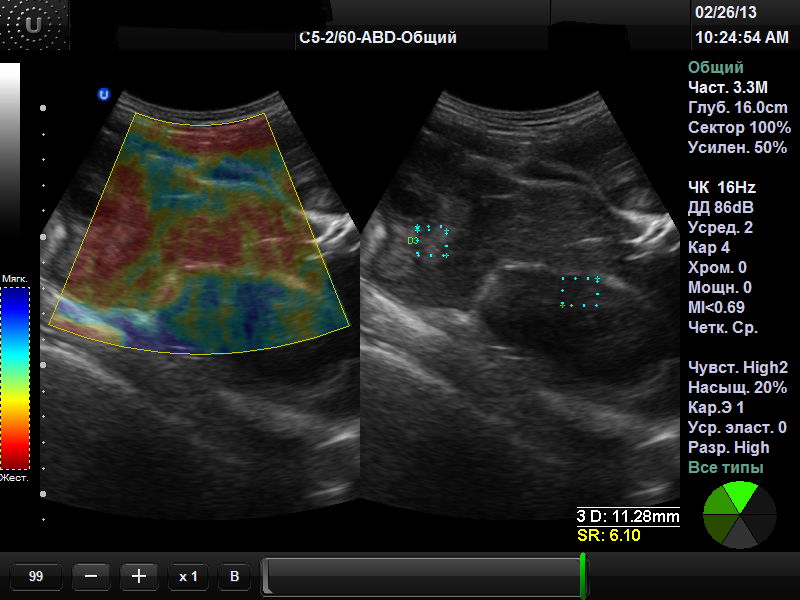
Рис. 5. RTE: множественные метастазы в печени Клинический случай 4. Женщина М., 48 лет, при УЗИ и КТ выявлены множественные очаги в печени неправильной формы, интерпретированные как метастазы. Однако, на RTE показатели ЕSR в диапазоне от 0,43 до 2,42, что свидетельствует в пользу множественных кавернозных гемангиом. Проведено тщательное обследование с привлечением лабораторно-инструментальных методов исследования – первичный очаг не обнаружен. Выполнена пункционная биопсия очагов транскутанным способом. Гистологического подтверждения злокачественного процесса не получено.
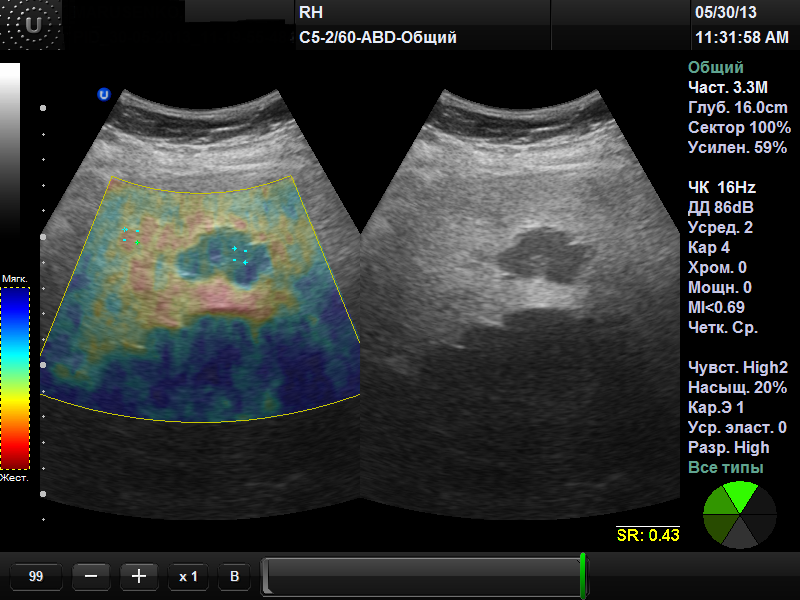
Рис. 6. RTE: множественные кавернозные гемангиомы печени Таким образом, первый опыт использования RTЕ позволяет считать эту методику необходимой в диагностике ФП, определении его стадии и прогнозировании течения заболеваний, особенно при невозможности проведения биопсии. Анализ параметров RTЕ является особенно полезным в динамике наблюдения за пациентами. Проведение дополнительного ультразвукового исследования в режиме RTЕ целесообразно для дифференциальной диагностики очаговых образований печени для точного представления об их характере и планирования дальнейшей врачебной тактики.
Литература 1. Sandrin L , Fourquet B , Hasquenoph JM, et al . Transient elastography: a new noninvasive method for assessment of hepatic fi brosis . Ultrasound Med Biol 2003 ; 29 ( 12 ): 1705 – 1713 . 2. Rifai K, Cornberg J, Bahr M, et al . ARFI elastography of the spleen is inferior to liver elastography for the detection of portal hypertension. / Ultraschall Med. 2011 Dec;32 Suppl 2:E24-30. doi: 10.1055/s-0031-1281771. Epub 2011 Dec 22. 3. Friedrich-Rust M , Ong MF , Herrmann E , et al . Real-time elastography for noninvasive assessment of liver fi brosis in chronic viral hepatitis . AJR Am J Roentgenol 2007 ; 188 ( 3 ): 758 – 764. 4. Jong Ho Chung, Hyung Su Ahn, Sang Gyune Kim et al. The usefulness of transient elastography, acoustic-radiation -force impulse elastography, and real-time elastography for the evaluation of liver fibrosis// Clinical and Molecular Hepatology. - 2013;19:156-164 5. Rizzo L, Calvaruso V, Cacopardo B, Alessi N, Attanasio M, Petta S, Fatuzzo F, Montineri A, Mazzola A, L'abbate L, Nunnari G, Bronte F, Di Marco V, Craxi A, Camma C. Comparison of transient elastography and acoustic radiation force impulse for non-invasive staging of liver fibrosis in patients with chronic hepatitis C. / Am J Gastroenterol. 2011 Dec;106(12):2112-20. 6. Sporea I, Sirli R, Popescu A, Bota S, Badea R, Lupsor M, Focsa M, Danila M. / Is it better to use two elastographic methods for liver fibrosis assessment? / World J Gastroenterol. 2011 Sep 7;17(33):3824-9. doi: 10.3748/wjg.v17.i33.3824 7. Morishita S, Hirooka Y, Sato K, et al. Real-time tissue elastography in chronic liver disease. Jpn J Clin Pathol 2010; 58:319–324. 8. Lupsor M, Badea R, Stefanescu H, Sparchez Z, Branda H, Serban A, Maniu A. / Performance of a new elastographic method (ARFI technology) compared to unidimensional transient elastography in the noninvasive assessment of chronic hepatitis C. Preliminary results. / J Gastrointestin Liver Dis. 2009 Sep;18(3):303-10. 9. Fujimoto K, Wada S, Oshita M et al: Non-invasive evaluation of Hepatic Fibrosis in patients with Chronic Hepatitis C using Elastography // Medix 2007;10 (suppl.): 24-27 10. Saftoiu A, Vilmann P, Hassan H, et al. Analysis of endoscopic ultrasound elastography used for characterization and differentiation of benign and malignant lymph nodes. Ultraschall Med 2006;27:535-42.